球磨工ブログ
カテゴリ:学校風景
2年生列車通学生清掃活動
学年末考査終了後、13~14時に人吉駅とひよどり越えの清掃が行われました。
年3回行っている清掃活動ですが、今回は2年生列車通学生が行いました。






清掃は真面目に行われていたのですが、生徒も私も気になったのが、3月15日より運行開始の新型車両「田園シンフォニー」で、試運転でホームに来ていました。(一般車両としての運行は3月8日からのようで、運行開始セレモニーもあるそうです。)




三両編成で、赤色の車両が「秋」、茶色の車両が「冬」、ベージュ色の車両が「春」となっていますが、「夏」はどこに?御存知の方、教えてください。
追記
来年度、青色の「夏」と白色の「朝霧」が納車される予定だそうです。
化学基礎
修学旅行、前期選抜などがあり、あまり授業が進んでいません。
でも、実験しない化学の授業はありえません。ということで、修学旅行後に実験しました。
でも、実験しない化学の授業はありえません。ということで、修学旅行後に実験しました。
実験12 酸・塩基の強弱
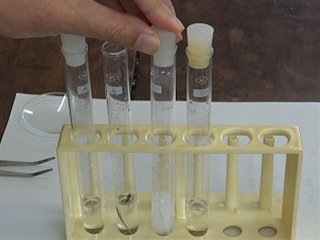
4本の試験管に入った塩酸、酢酸、水酸化ナトリウム水溶液、アンモニア水を判別する実験です。
まずは、においから。どの溶液も同じモル濃度ですが、十分に薄めてあるため、ほとんどの班が酢酸しか判断することができません。数名の生徒はアンモニア水を嗅ぎ分けました。よい鼻の持ち主です。
(経験上の話となりますが、酢酸はかなり希釈してもにおいが分かりますが、アンモニアはある程度希釈するとにおいが分かりにくくなります。)
次は、リトマス紙で酸性かアルカリ性かを判断します。
溶液をガラス棒につけ、赤と青のリトマス紙につけて変化を見ます。




次は万能指示薬で溶液のpHを調べます。pH7は中性、7より小さいと酸性、7より大きいと塩基性(アルカリ性)です。




pHを決定したことで、4種類の溶液が何であるか判断できました。
pHの大小関係 塩酸<酢酸<7<アンモニア水<水酸化ナトリウム水溶液
さらに、塩酸と酢酸について、酸の強弱を観察するためにマグネシウムリボンを入れ、気体の発生の激しさを比較します。また、気体の種類を調べるため、燃焼させます。
燃焼時の音と試験管が曇り水ができたことから、気体は水素であることが分かります。
今回の実験では、同じ濃度の強酸、弱酸、強塩基、弱塩基の水溶液4種類の組み合わせだったので、万能指示薬で判別できました。
例えば、強酸が2種類入っていれば、同じ実験結果となるため判別できません。(別の方法で判別します。)
金属と酸の組み合わせによっては、気体が発生しなかったり、水素以外の気体が発生することもあります。一般的な組み合わせでは、水素が発生することを理解しておきましょう。
校舎(村山公園より)
早朝、村山公園から球磨工を見ると・・・見えない。霧が深い。
しばらく、時間をおいて再び来て、見たところぼんやり見えました。
しばらく、時間をおいて再び来て、見たところぼんやり見えました。
朝の村山公園です。この霧の向こうに球磨工はあります。

見えますか?

もう少し、拡大してみました。

プレハブの撤去、ロータリーの工事も終わり、村山公園から外観を取りたかったのですが、霧にはばまれました。もっと天気の良い、昼間に撮影し直したいと思います。
化学基礎
ま、まずい。ネタがない!
こんなときは、我が身を切って対応しないと・・・ということで、化学基礎の実験です。
こんなときは、我が身を切って対応しないと・・・ということで、化学基礎の実験です。
1月、授業は酸と塩基(アルカリ)に入りました。実験は修学旅行から帰ってきてから進める予定です。
12月中旬は、化学式の復習を行いながら、金属銀をつくる実験を行いました。
実験11 金属樹と銀鏡反応
金属樹の実験はとても簡単です。
今回の実験では、無色の硝酸銀水溶液に、銅(銅線)を入れて、待つだけです。
実験の前に、銀イオン、硝酸イオンの化学式(イオン式)を書き、それらを組み合わせて、硝酸銀の化学式(組成式)を書きました。
実験は時間がかかりますが、しばらく待つと木の枝のような銀ができます。

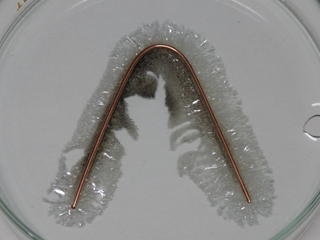


50分の授業時間では銀の成長は限られたものとなりますが、反応時間を長くすると、溶液中の銀イオンがどんどん金属銀に変化し、少しですが長く、太い銀になります。

写真では見えにくいですが、この反応で溶液は徐々に青色に変化します。青色の原因は、銅(II)イオンです。銀イオンが銀に変化し、銅が銅(II)イオンに変化するという、イオンと金属の入れ替えが起こります。
詳しい内容は、2月の授業(酸化還元反応)で学習します。
次は銀鏡反応です。
硝酸銀水溶液にアンモニア水を加えると、酸化銀ができ、褐色に濁ります。酸化銀は多量のアンモニア水には溶けてしまうので、ちょうど溶けるまでアンモニア水を加え、さらにブドウ糖(グルコース)水溶液を加え、温めると容器の内側に銀ができます。
実験の前に、アンモニア分子の電子式、構造式、分子式と形を書き、分子の復習をしました。
硝酸銀水溶液にアンモニア水を加えます。
酸化物を燃やさずにつくることができる点も不思議ではないですか?


アンモニア水をさらに加え、褐色の酸化銀が溶けたら、ブドウ糖水溶液を加えます。


温めると銀が出てきます。
無色の液体から銀ができる様子は感動です。


正しい説明ではありませんが、これまで学習した知識で説明するのであれば、溶けた酸化銀が還元されて銀になったと考えることができます。
ブドウ糖は血中にもある大切な糖類ですが、甘いという特徴だけでなく、相手を還元する性質も持っており、今回の実験では酸化銀を銀に還元する役割として加えられました。
暖房がなく、室温が氷点下になる日もある化学実験室ですが、生徒は暖かい教室での座学より、極寒の化学室での実験を求めております。
しっかり防寒対策をして、3学期も楽しく実験しましょう。
工事(ロータリー周辺)
冬休み中も校内の工事は引き続き行われています。
12月27日の様子
駐輪場前(仮設の事務室・校長室)ではアスファルト舗装が行われていました。


アスファルトフィニッシャ:アスファルト舗装のために使われる建設機械です。今回の工事で使用されているのは小型のミニアスファルトフィニッシャと思います。


ロードローラーはタンデム式とハンドガイド式の2台がありました。


12月30日の様子
駐輪場前は駐車場になりました。また駐車場とロータリーの段差も解消されました。


次の工事はどこかな?
行事予定表
球磨工公式インスタグラム
球磨工の情報を発信中!
リンクはこちらから
リンク
6
1
0
3
4
3
9
学校情報
〒868‐8515
熊本県人吉市城本町800番地
TEL 0966-22-4189
FAX 0966-22-5049
E-mail
kuma-th@pref.kumamoto.lg.jp
熊本県教育情報システム
登録機関
管理責任者 校長 坂本道彦
運用担当者 ホームページ係
リンク
カレンダー
| 日 | 月 | 火 | 水 | 木 | 金 | 土 |
26 | 27 | 28 | 29 | 30 | 1 | 2 |
3 | 4 | 5 | 6 | 7 | 8 | 9 |
10 | 11 | 12 | 13 | 14 | 15 | 16 |
17 | 18 | 19 | 20 | 21 | 22 | 23 |
24 | 25 | 26 | 27 | 28 | 29 | 30 |
31 | 1 | 2 | 3 | 4 | 5 | 6 |