球磨工ブログ
カテゴリ:学校風景
化学基礎
ま、まずい。ネタがない!
こんなときは、我が身を切って対応しないと・・・ということで、化学基礎の実験です。
こんなときは、我が身を切って対応しないと・・・ということで、化学基礎の実験です。
1月、授業は酸と塩基(アルカリ)に入りました。実験は修学旅行から帰ってきてから進める予定です。
12月中旬は、化学式の復習を行いながら、金属銀をつくる実験を行いました。
実験11 金属樹と銀鏡反応
金属樹の実験はとても簡単です。
今回の実験では、無色の硝酸銀水溶液に、銅(銅線)を入れて、待つだけです。
実験の前に、銀イオン、硝酸イオンの化学式(イオン式)を書き、それらを組み合わせて、硝酸銀の化学式(組成式)を書きました。
実験は時間がかかりますが、しばらく待つと木の枝のような銀ができます。

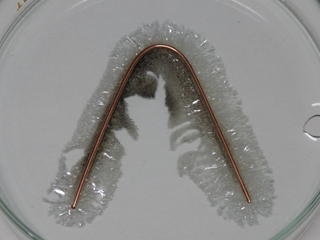


50分の授業時間では銀の成長は限られたものとなりますが、反応時間を長くすると、溶液中の銀イオンがどんどん金属銀に変化し、少しですが長く、太い銀になります。

写真では見えにくいですが、この反応で溶液は徐々に青色に変化します。青色の原因は、銅(II)イオンです。銀イオンが銀に変化し、銅が銅(II)イオンに変化するという、イオンと金属の入れ替えが起こります。
詳しい内容は、2月の授業(酸化還元反応)で学習します。
次は銀鏡反応です。
硝酸銀水溶液にアンモニア水を加えると、酸化銀ができ、褐色に濁ります。酸化銀は多量のアンモニア水には溶けてしまうので、ちょうど溶けるまでアンモニア水を加え、さらにブドウ糖(グルコース)水溶液を加え、温めると容器の内側に銀ができます。
実験の前に、アンモニア分子の電子式、構造式、分子式と形を書き、分子の復習をしました。
硝酸銀水溶液にアンモニア水を加えます。
酸化物を燃やさずにつくることができる点も不思議ではないですか?


アンモニア水をさらに加え、褐色の酸化銀が溶けたら、ブドウ糖水溶液を加えます。


温めると銀が出てきます。
無色の液体から銀ができる様子は感動です。


正しい説明ではありませんが、これまで学習した知識で説明するのであれば、溶けた酸化銀が還元されて銀になったと考えることができます。
ブドウ糖は血中にもある大切な糖類ですが、甘いという特徴だけでなく、相手を還元する性質も持っており、今回の実験では酸化銀を銀に還元する役割として加えられました。
暖房がなく、室温が氷点下になる日もある化学実験室ですが、生徒は暖かい教室での座学より、極寒の化学室での実験を求めております。
しっかり防寒対策をして、3学期も楽しく実験しましょう。
行事予定表
球磨工公式インスタグラム
球磨工の情報を発信中!
リンクはこちらから
リンク
6
1
0
4
2
7
3
学校情報
〒868‐8515
熊本県人吉市城本町800番地
TEL 0966-22-4189
FAX 0966-22-5049
E-mail
kuma-th@pref.kumamoto.lg.jp
熊本県教育情報システム
登録機関
管理責任者 校長 坂本道彦
運用担当者 ホームページ係
リンク
カレンダー
| 日 | 月 | 火 | 水 | 木 | 金 | 土 |
26 | 27 | 28 | 29 | 30 | 1 | 2 |
3 | 4 | 5 | 6 | 7 | 8 | 9 |
10 | 11 | 12 | 13 | 14 | 15 | 16 |
17 | 18 | 19 | 20 | 21 | 22 | 23 |
24 | 25 | 26 | 27 | 28 | 29 | 30 |
31 | 1 | 2 | 3 | 4 | 5 | 6 |