球磨工ブログ
化学基礎
今年度、最後の化学実験は電気分解となりました。
中学校でも学習・実験する水の電気分解です。
中学校でも学習・実験する水の電気分解です。
実験18 電気分解
まずは電気分解について学習し、実験に入りました。
水酸化ナトリウム水溶液の電気分解を行うための準備から始めます。
注射器でつくった電極に水溶液を満たし、ビーカーに立て、電源につないで電気分解を始めます。




電源を買うことも、電池を買うこともできないので、手回し発電機による電気分解です。一人一分、四人で四分間の電気分解を行いました。


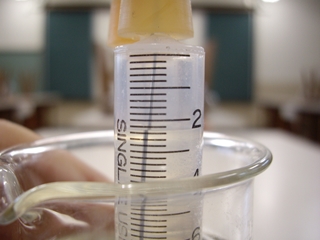
電源や電池の便利さやすばらしさを体感するだけではなく、生成物の確認も行います。陰極の水素が5.4+0.5=5.9mL、陽極の酸素が2.3+0.5=2.8mL(注射器の上部に目盛りのない0.5mLの空間があるため、目盛りの読み取り値に0.5mLを足しています。)
5.9÷2.8≒2.1 水素:酸素=2.1:1となり、学習する2:1に近い結果となりました。

次は電極を芯を出した鉛筆に変えて、水酸化ナトリウム水溶液を電気分解しますが、15秒~1分程度電気分解した後に電源を外し、電子メロディにつなぎ替えます。


電気分解も充電も、相手に電流を流すため同じことと考えることができます。水酸化ナトリウム水溶液の電気分解(充電)でできた電池は水素(と酸素)を燃料として働く燃料電池です。
行事予定表
球磨工公式インスタグラム
球磨工の情報を発信中!
リンクはこちらから
リンク
6
1
0
1
2
0
1
学校情報
〒868‐8515
熊本県人吉市城本町800番地
TEL 0966-22-4189
FAX 0966-22-5049
E-mail
kuma-th@pref.kumamoto.lg.jp
熊本県教育情報システム
登録機関
管理責任者 校長 坂本道彦
運用担当者 ホームページ係
リンク
カレンダー
| 日 | 月 | 火 | 水 | 木 | 金 | 土 |
26 | 27 | 28 | 29 | 30 | 1 | 2 |
3 | 4 | 5 | 6 | 7 | 8 | 9 |
10 | 11 | 12 | 13 | 14 | 15 | 16 |
17 | 18 | 19 | 20 | 21 | 22 | 23 |
24 | 25 | 26 | 27 | 28 | 29 | 30 |
31 | 1 | 2 | 3 | 4 | 5 | 6 |